Grafito
| Grafito | ||
|---|---|---|
 Grafito | ||
| General | ||
| Categoría | Minerales elementos nativos | |
| Clase | 1.CB.05a (Strunz) | |
| Fórmula química | C | |
| Propiedades físicas | ||
| Color | Negro acero y gris | |
| Raya | Negra | |
| Lustre | metálica, tierra | |
| Transparencia | no | |
| Sistema cristalino | Hexagonal (6/m 2/m 2/m) | |
| Hábito cristalino | Tabular, de seis caras foliada, las masas granulares compactados | |
| Exfoliación | Perfecto en una dirección | |
| Fractura | Escamosa, de lo contrario en bruto, cuando no en la división | |
| Dureza | 1-2 (Mohs) | |
| Tenacidad | Escamas finas flexibles y quebradizas | |
| Densidad | 2,09 a 2,23 g/cm³ | |
| Índice de refracción | Opaco | |
| Pleocroísmo | No | |
| Solubilidad | Fundido Ni | |
| Magnetismo | diamagnético | |
| [editar datos en Wikidata] | ||
El grafito es una de las formas alotrópicas en las que se puede presentar el carbono junto al diamante, los fulerenos, losnanotubos y el grafeno. A presión atmosférica y temperatura ambiente es más estable el grafito que el diamante, sin embargo la descomposición del diamante es tan extremadamente lenta que sólo es apreciable a escala geológica.
Fue nombrado por Abraham Gottlob Werner en el año 1789. El término grafito deriva del griego γραφειν (graphein) que significa "escribir", ya que se usa principalmente para crear la punta de los lápices. También se denomina plumbagina y plomo negro.
Puede extraerse de yacimientos naturales , pero también se produce artificialmente. El principal productor mundial de grafito esChina, seguido de India y Brasil.
Índice
[ocultar]Estructura[editar]
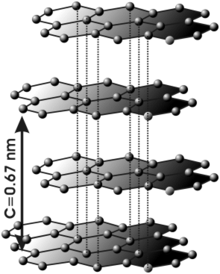
En el grafito los átomos de carbono presentan hibridación sp2, esto significa que forma tres enlaces covalentes en el mismo plano a un ángulo de 120º (estructura hexagonal) y que un orbital Π perpendicular a ese plano quede libre (estos orbitales deslocalizados son fundamentales para definir el comportamiento eléctrico del grafito). El enlace covalente entre los átomos de una capa es extremadamente fuerte, sin embargo las uniones entre las diferentes capas se realizan por fuerzas de Van der Waals e interacciones entre los orbitales Π, y son mucho más débiles.
Se podría decir que el grafito está constituido por capas de grafeno superpuestas.
Esta estructura laminar hace que el grafito sea un material marcadamente anisótropo.
Al igual que el diamante, el grafito está constituido exclusivamente por átomos de carbono, pero con una estructura cristalina particular. Tanto el grafito como el diamante son formas alotrópicas del carbono, de entre las múltiples que son posibles. El grafito, como el diamante, es un mineral semimetálico. Se conocen procesos mediante los cuales el grafito puede convertirse en diamante mediante el uso de muy elevadas presiones y temperaturas, pero esos métodos son de un coste superior al valor de mercado de los diamantes que se obtendrían, por lo que el hecho apenas se ha aprovechado comercialmente excepto para fabricar microdiamantes empleados en herramientas especiales.
Propiedades[editar]
El grafito es de color negro con brillo metálico, refractario y se exfolia con facilidad. En la dirección perpendicular a las capas presenta una conductividad de la electricidad baja y que aumenta con la temperatura, comportándose pues como un semiconductor. A lo largo de las capas la conductividad es mayor y aumenta proporcionalmente a la temperatura, comportándose como un conductor semimetálico. Aunque tanto el grafito como el diamante están formados exclusivamente por átomos de carbono, el grafito es muy blando y opaco, mientras que el diamante es el mineral más duro según la escala de Mohs y además deja pasar la luz a través de si, estas marcadas diferencias físicas se deben exclusivamente a las diferentes redes cristalinas o retículos sobre las que se disponen los átomos de carbono en el grafito (átomos de carbono en los vértices de prismas hexagonales) y en el diamante (la red cristalina está hecha de tetraedros regulares cuyos vértices son átomos de carbono).
Aplicaciones[editar]
- El grafito mezclado con una pasta se utiliza para fabricar la mina de los lápices.
- El grafito se emplea en ladrillos, crisoles, etc.
- Al deslizarse las capas fácilmente en el grafito, resulta ser un buen lubricante sólido.
- Se utiliza en la fabricación de diversas piezas en ingeniería, como pistones, juntas, arandelas, rodamientos, etc.
- Este material es conductor de la electricidad y se usa para fabricar electrodos. También tiene otras aplicaciones eléctricas, como los carbones de un motor (escobillas), que entran en contacto con el colector.
- Se emplea en reactores nucleares, como moderadores y reflectores.
- Es usado para crear discos de grafito parecidos a los de discos vinilo salvo por su mayor resistencia a movimientos bruscos de las agujas lectoras.
- Se puede crear Grafeno, material de alta conductividad eléctrica y térmica, futuro sustituto del silicio en la fabricación de chips.
- Se emplea en la fabricación de carretes y cañas de pesca.
ResponderEliminar3°"B"
Al igual que la anterior lectura, ésta también me pareció interesante ya que menciona y/o informa sobre las características del grafito; así como su estructura y sus propiedades, como también de las aplicaciones que se obtiene del grafito.
En concreto quiero decir con respecto a éstas dos lecturas que son muy interesantes, pues mediante una buena lectura y un análisis, se puede llegar a encender los temas propuestos como es el caso de la lectura del diamante y el grafito.
Muchas gracias por estas informaciones profesor, me ayudan a ampliar más mis conocimientos.
3°"B"
ResponderEliminarEsta lectura me pareció interesante ya que nos explica un poco mas sobre el grafito que es una de las formas alotrópicas en las que se puede presentar el carbono junto al diamante, los fulerenos, losnanotubos y el grafeno.Tambien nos explica las detalladas caracteristicas que tiene en los que esta incluidos las aplicaciones y propiedades.
3D
ResponderEliminaresta lectura me parecio bien ya que nos enseña sobre el grafito sus estructuras propiedades sus aplicaciones tambien que son unas de la formas en las que el carbonoy el diamante presentan tambien sus caracteristicas
3° B
ResponderEliminarEsta lectura explica sobre el grafito que es una de las formas alotrópicas en las que se puede presentar el carbono junto al diamante. A presión atmosférica y temperatura ambiente es más estable el grafito que el diamante.Explica su estructura,propiedades y aplicaciones.
3°C
ResponderEliminarEsta lectura me pareció muy interesante pues pude entender la importancia del grafito,que al igual que el diamante esta formado exclusivamente de carbono,el grafito es mucho mas blando y opaco,es un mineral semimetálico. Se conoce que el grafito se puede convertir en diamante ,mediante una serie de procesos que implican el uso de muy elevedas presiones y temperaturas,pero estos métodos cuestan mucho ,aún más que el costo del valor del diamante en el mercado.
Tiene muchos usos,pues al mezclarse con una pasta se pueden crear las puntas de los lápices,siendo el mayor productor de grafito,CHINA,
Me servirá de mucho para ampliar mis conocimientos y responder las tareas propuestas.
3´´A´´
ResponderEliminaresta lectura es interesante porque nos explica un poco mas sobre el grafito que es una de las formas alotrópicas en las que se puede presentar el carbono junto al diamante,la importancia del grafito,que al igual que el diamante esta formado exclusivamente de carbono,el grafito es mucho mas blando y opaco,es un mineral semimetálico.
EL VIDEO NOS HABLA SOBRE EL GRAFITO, NOS DICE QUE ES MAS ESTABLE QUE EL DIAMANTE, ESTA COMPUESTO POR CARBONO Y MAYOR MENTE ES UTILIZADO EN LOS LAPICES,SU SISTEMA CRISTALINO ES HEXAGONAL. GRACIAS PROFE. EL VIDEO ESTUVO MUY INTERESANTE. 3º "A"
ResponderEliminar3B
ResponderEliminarEsta lectura me pareció muy interesante pues pude entender la importancia del grafito,que al igual que el diamante esta formado exclusivamente de carbono,el grafito es mucho mas blando y opaco,es un mineral semimetálico.
3"B"
ResponderEliminarEste texto me pareció interesante ya que me ayudo a entender muy bien todo sobre el grafito y sus características principales y que es una forma alotrópica del carbono y que es de un color negro con brillo metalico
3°"B"
ResponderEliminarLa lectura nos brinda mucha informacion acerca del GRAFITO, del cual sabemos que es una de las formas alotrópicas en las que se puede presentar el carbono junto al diamante( del que se hablo en el video pasado).
Nos dice que el gafito tiene una estructura de C= 0.67 nm y es de color negro acero y gris.Tambien menciona sus aplicaciones y propiedades.
ESTUVO INTERESANTE E INFORMATIVA.
3°C
ResponderEliminaresta lectura me parece muy interesante a igual que la otra porque en esta lectura nos explica las características del grafito; también como es su estructura , sus propiedades, como también los productos que se obtiene del grafito.
3A
ResponderEliminarEl video me parecio muy interesante ya que nos habla acerca del grafito el cual es un mineral,tambien nos habla acerca de su Estructura, sus Propiedades, sus Aplicaciones, sus Compuestos de intercalación de grafito entre otras cosas igual de interesantes
kristel quispe 3°B
ResponderEliminarme parecio muy interesante este texto k habla sobre el grafito su composicion, estructura atomica , sus propiedades :El grafito es de color negro con brillo metálico,
la lectura me parecio muy interesante ya que nos da a entender sobre el grafito lo cual en un mineral sobre su estructura y sus propiedades
ResponderEliminar3 "B"
ResponderEliminarLa información fue de gran ayuda para mi exposicion, gracias
3 "A"
ResponderEliminareste texto o información me sirvió mucho de ayuda ya que me enseño mas sobre las características del grafito, como su estructura y sus propiedades así como las aplicaciones que se obtiene del grafito también nos explica las detalladas características que tiene en los que esta incluidos las aplicaciones y propiedades.
3'D'
ResponderEliminarEste texto nos habla sobre el grafito otra forma alotropica del carbono nos dice que es más estable que el diamante de color negro acero y gris conduce electricidad y esta aumenta con la temperatura ademas se encuentra en el lapiz en el ladrillo y hasta en los chips
es semimetalico y con procesos especiales se puede llegar a combertir en diamante
3°C
ResponderEliminarEsta lectura me parecio interesante ya que nos enseña sobre el grafito sus estructuras propiedades sus aplicaciones ,tambien que son unas de la formas en las que el carbono y el diamante presentan sus caracteristicas.
3°A
ResponderEliminarla información nos enseña sobre el grafito cuales son sus propiedades aplicaciones y datos generales.
3B MARJORIE ALVARADO
ResponderEliminarme parecio interesante la lectura, etc
En la información nos habla sobre el grafito, nos habla sobre la estructura del grafito y que es mas estable que el diamante y mas blando y opaco, nos habla también de sus propiedades y aplicaciones que se pueden dar del grafito, es de color negro y gris.
ResponderEliminar3ro"A"
3°"D"Esta informacion nos enseña sobre el grafito que es una forma alotropica del carbon ,es un mineral de color negro con brillo metalico,este tiene un gran uso en la vida cotidiana.
ResponderEliminar3 D
ResponderEliminarLa información nos habla sobre el grafito, entendí que es una forma alotrópica, se presenta el carbono junto al diamante, los fulerenos, los nanotubos y el grafeno. El grafito es de color negro con brillo metálico. Este material es conductor de la electricidad y se usa para fabricar electrodos. También tiene otras aplicaciones eléctricas, como los carbones de un motor, que entran en contacto con el colector.
3° "B"
ResponderEliminarEste texto nos habla del grafito....es cual nos ayudara para el trabajo que nos había dejado.
3° "B"
ResponderEliminarEste texto nos habla del grafito....es cual nos ayudara para el trabajo que nos había dejado.
me parecio interesante ya que nos enseña sobre el grafito sus estructuras propiedades sus aplicaciones
ResponderEliminar3ºC
ResponderEliminaresta lectura me parece muy interesante porque nos explica las características del grafito; también como es su estructura y sus propiedades
3ºC
ResponderEliminaresta lectura me parece muy interesante porque nos explica las características del grafito; también como es su estructura y sus propiedades
muy interesante la lectura acerca del grafito sabre que El grafito es una de las formas alotrópicas en las que se puede presentar el carbono junto al diamante, los fulerenos, losnanotubos y el grafeno.
ResponderEliminar