miércoles, 16 de diciembre de 2015
martes, 15 de diciembre de 2015
EXAMEN FINAL
EVALUACION
FINAL DE TERCER AÑO PERIODO 2015-12-15 JCE
I-
ESCRIBA EN EL PARENTESIS DE LA DERECHA LA
LETRA QUE LE CORRESPONDE.
a) MgO () Gira alrededor
del núcleo
b) NaOH () aldehído
c) HCl () amida
d) p+ () éter
e) C=C () protón
f)
R-OH
() hidróxido de sodio
g) R-NH2
() óxido de magnesio
h) R-O-R” () ácido muriático o clorhídrico
i)
R-COOH
() doble enlace
j)
R-CO-NH2
() amina
k) R-COO-R”
() ácido orgánico
l)
R-CHO
() éster
m) R-CO-R”
() alcohol
n) e- () cetona
II-RESPONDA LAS SIGUIENTES AFIRMACIONES Y SEÑALE LA RESPUESTA CORRECTA.
1. Actualmente los electrones
forman una nube electrónica que está conformado por:
a) Niveles b) subniveles
c) orbitales d) todos.
2. Sirven para quitar los
óxidos de los metales:
a) Ácidos b) hidróxidos
c) todos d) ningunos
3. los enlaces químicos son los
responsables de la unión de:
a) átomos b) la formación de moléculas c) todas
d) mezclas
4.Son hidrocarburos todas las
sustancias formadas por:
a) C y O b) C y H
c) C,H y O d) ninguno
5. El polivinilo es un hidrocarburo formado por la polimerización del:
a) alcano b) eteno
c) etino d) todos
6. El metanol es un veneno que:
a) mata neuronas b) deja ciego
c) causa la muerte d)todas
7.El formol es un:
a) aldehído b) cetona
c) acido orgánico d) éter
8.El ácido fórmico en forma natural lo produce:
a) el gusano b) hormiga
c) mosquito d) ninguno
9.El olor a pescado es por la presencia de :
a) aminas b)amidas
c) esteres d) éteres
10.El olor de alas frutas es por
los:
a) ácidos orgánicos b) esteres
c)aminas d) ninguno
11. Antiguamente se utilizó como anestésico en las intervenciones quirúrgicas:
a) silocaina b) etiloxietil c) éter dietílico d) ninguno
12. Es el ladrillo en la construcción de las proteínas:
a) amino b) aminoácido
c)monosacáridos d) triglicéridos
13.La electricidad es producido por la liberación de:
a) protones b) electrones
c) neutrones d) todos
¡SUERTE!
SEA ESTA NAVIDAD UN MOMENTO DE PAZ, FELICIDAD Y DE REFLEXION EN FAMILIA
DE LO QUE HICIMOS Y DE LO QUE DEBIMOS HACER Y EL AÑO PRÓXIMO SEA DE PROSPERIDAD Y DE RECTIFICACIÓN DE TODOS
NUESTROS ERRORESK
¡ FELIZ NAVIDAD ESTIMADOS
ESTUDIANTES!
lunes, 14 de diciembre de 2015
viernes, 4 de diciembre de 2015
UNIDADES FUNDAMENTALES EN LA CONSTRUCCIÓN DELAS PROTEINAS: LOS AA
Aminoácidos esenciales
Se llaman aminoácidos esenciales aquellos que no pueden ser sintetizados en el organismo y para obtenerlos es necesario tomar alimentos ricos en proteínas que los contengan. Nuestro organismo, descompone las proteínas para obtener los aminoácidos esenciales y formar así nuevas proteínas.
Histidina
Este aminoácido se encuentra abundantemente en la hemoglobina y se utiliza en el tratamiento de la artritis reumatoide, alergias, úlceras y anemia. Es esencial para el crecimiento y la reparación de los tejidos. La Histidina, también es importante para el mantenimiento de las vainas de mielina que protegen las células nerviosas, es necesario para la producción tanto de glóbulos rojos y blancos en la sangre, protege al organismo de los daños por radiación, reduce la presión arterial, ayuda en la eliminación de metales pesados del cuerpo y ayuda a mejorar la líbido.
Isoleucina
La Isoleucina es necesaria para la formación de hemoglobina, estabiliza y regula el azúcar en la sangre y los niveles de energía. Este aminoácido es valioso para los deportistas porque ayuda a la curación y la reparación del tejido muscular, piel y huesos. La cantidad de este aminoácido se ha visto que es insuficiente en personas que sufren de ciertos trastornos mentales y físicos.
Leucina
La leucina interactúa con los aminoácidos isoleucina y valina para promover la cicatrización del tejido muscular, la piel y los huesos y se recomienda para quienes se recuperan de la cirugía. Este aminoácido reduce los niveles de azúcar en la sangre y ayuda a aumentar la producción de la hormona del crecimiento.
Lisina
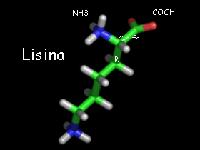
Funciones de este aminoácido son garantizar la absorción adecuada de calcio y mantiene un equilibrio adecuado de nitrógeno en los adultos. Además, la lisina ayuda a formar colágeno que constituye el cartílago y tejido conectivo. La Lisina también ayuda a la producción de anticuerpos que tienen la capacidad para luchar contra el herpes labial y los brotes de herpes y reduce los niveles elevados de triglicéridos en suero.
Metionina
La Metionina es un antioxidante de gran alcance y una buena fuente de azufre, lo que evita trastornos del cabello, piel y uñas, ayuda a la descomposición de las grasas, ayudando así a prevenir la acumulación de grasa en el hígado y las arterias, que pueden obstruir el flujo sanguíneo a el cerebro, el corazón y los riñones, ayuda a desintoxicar los agentes nocivos como el plomo y otros metales pesados, ayuda a disminuir la debilidad muscular, previene el cabello quebradizo, protege contra los efectos de las radiaciones, es beneficioso para las mujeres que toman anticonceptivos orales, ya que promueve la excreción de los estrógenos, reduce el nivel de histamina en el cuerpo que puede causar que el cerebro transmita mensajes equivocados, por lo que es útil a las personas que sufren de esquizofrenia.
Fenilalanina
Aminoácidos utilizados por el cerebro para producir la noradrenalina, una sustancia química que transmite señales entre las células nerviosas en el cerebro, promueve el estado de alerta y la vitalidad. La Fenilalanina eleva el estado de ánimo, disminuye el dolor, ayuda a la memoria y el aprendizaje, que se utiliza para tratar la artritis, depresión, calambres menstruales, las jaquecas, la obesidad, la enfermedad de Parkinson y la esquizofrenia.
Treonina
La treonina es un aminoácido cuyas funciones son ayudar a mantener la cantidad adecuada de proteínas en el cuerpo, es importante para la formación de colágeno, elastina y esmalte de los dientes y ayuda a la función lipotrópica del hígado cuando se combina con ácido aspártico y la metionina, previene la acumulación de grasa en el hígado, su metabolismo y ayuda a su asimilación.
Triptofano
Este aminoácido es un relajante natural, ayuda a aliviar el insomnio induciendo el sueño normal, reduce la ansiedad y la depresión y estabiliza el estado de ánimo, ayuda en el tratamiento de la migraña, ayuda a que el sistema inmunológico funcione correctamente. El Triptofano ayuda en el control de peso mediante la reducción de apetito, aumenta la liberación de hormonas de crecimiento y ayuda a controlar la hiperactividad en los niños.
Valina
La Valina es necesaria para el metabolismo muscular y la coordinación, la reparación de tejidos, y para el mantenimiento del equilibrio adecuado de nitrógeno en el cuerpo, que se utiliza como fuente de energía por el tejido muscular. Este aminoácido es útil en el tratamiento de enfermedades del hígado y la vesícula biliar, promueve el vigor mental y las emociones tranquilas.
Alanina
Desempeña un papel importante en la transferencia de nitrógeno de los tejidos periféricos hacia el hígado, ayuda en el metabolismo de la glucosa, un carbohidrato simple que el cuerpo utiliza como energía, protege contra la acumulación de sustancias tóxicas que se liberan en las células musculares cuando la proteína muscular descompone rápidamente para satisfacer las necesidades de energía, como lo que sucede con el ejercicio aeróbico, fortalece el sistema inmunológico mediante la producción de anticuerpos.
Aminoácidos no esenciales
Los aminoácidos no esenciales son aquellos que pueden ser sintetizados en el organismo a partir de otras sustancias.
Arginina
Este aminoácido está considerado como "El Viagra Natural" por el aumento del flujo sanguíneo hacia el miembro viril, retrasa el crecimiento de los tumores y el cáncer mediante el refuerzo del sistema inmunológico, aumenta el tamaño y la actividad de la glándula del timo, que fabrica las células T, componentes cruciales del sistema inmunológico. La Arginina, ayuda en la desintoxicación del hígado neutralizando el amoniaco, reduce los efectos de toxicidad crónica de alcohol, que se utiliza en el tratamiento de la esterilidad en los hombres, aumentando el conteo de espermatozoides; ayudas en la pérdida de peso, ya que facilita un aumento de masa muscular y una reducción de grasa corporal, ayuda a la liberación de hormonas de crecimiento, que es crucial para el "crecimiento óptimo" músculo y la reparación de tejidos, es un componente importante del colágeno que es bueno para la artritis y trastornos del tejido conectivo y ayuda a estimular el páncreas para que libere insulina.
Ácido Aspártico
El Ácido Aspártico aumenta la resistencia y es bueno para la fatiga crónica y la depresión, rejuvenece la actividad celular, la formación de células y el metabolismo, que le da una apariencia más joven, protege el hígado, ayudando a la expulsión de amoniaco y se combina con otros aminoácidos para formar moléculas que absorben las toxinas y sacarlas de la circulación sanguínea. Este aminoácido también ayuda a facilitar la circulación de ciertos minerales a través de la mucosa intestinal, en la sangre y las células y ayuda a la función del ARN y ADN, que son portadores de información genética.
Cisteína
La Cisteína funciona como un antioxidante de gran alcance en la desintoxicación de toxinas dañinas. Protege el cuerpo contra el daño por radiación, protege el hígado y el cerebro de daños causados por el alcohol, las drogas y compuestos tóxicos que se encuentran en el humo del cigarrillo, se ha utilizado para tratar la artritis reumatoide y el endurecimiento de las arterias. Otras funciones de este aminoácido es promover la recuperación de quemaduras graves y la cirugía, promover la quema de grasa y la formación de músculos y retrasar el proceso de envejecimiento. La piel y el cabello se componen entre el 10% y el 14% de este aminoácido.
Ácido Glutámico
El Ácido Glutámico actúa como un neurotransmisor excitatorio del sistema nervioso central, el cerebro y la médula espinal. Es un aminoácido importante en el metabolismo de azúcares y grasas, ayuda en el transporte de potasio en el líquido cefalorraquídeo, actúa como combustible para el cerebro, ayuda a corregir los trastornos de personalidad, y es utilizado en el tratamiento de la epilepsia, retraso mental, distrofia muscular y úlceras.
Glutamina
Es el aminoácido más abundante en los músculos. La Glutamina ayuda a construir y mantener el tejido muscular, ayuda a prevenir el desgaste muscular que puede acompañar a reposo prolongado en cama o enfermedades como el cáncer y el SIDA. Este aminoácido es un "combustible de cerebros" que aumenta la función cerebral y la actividad mental, ayuda a mantener el equilibrio del ácido alcalino en el cuerpo, promueve un sistema digestivo saludable, reduce el tiempo de curación de las úlceras y alivia la fatiga, la depresión y la impotencia, disminuye los antojos de azúcar y el deseo por el alcohol y ha sido usado recientemente en el tratamiento de la esquizofrenia y la demencia.
Glicina
La Glicina retarda la degeneración muscular, mejora el almacenamiento de glucógeno, liberando así a la glucosa para las necesidades de energía, promueve una próstata sana, el sistema nervioso central y el sistema inmunológico. Es un aminoácido útil para reparar tejidos dañados, ayudando a su curación.
Ornitina
Este aminoácido ayuda a pedir la liberación de hormonas de crecimiento, lo que ayuda al metabolismo de la grasa corporal (este efecto es mayor si se combina con la arginina y carnitina), es necesario para un sistema inmunológico saludable, desintoxica el amoniaco, ayuda en la regeneración del hígado y estimula la secreción de insulina. La Ornitina también ayuda a que la insulina funcione como una hormona anabólica ayudando a construir el músculo.
Prolina
Funciones de este aminoácido son mejorar la textura de la piel, ayudando a la producción de colágeno y reducir la pérdida de colágeno a través del proceso de envejecimiento. Además, la Prolina ayuda en la cicatrización del cartílago y el fortalecimiento de las articulaciones, los tendones y los músculos del corazón. La Prolina trabaja con la vitamina C para ayudar a mantener sanos los tejidos conectivos.
Serina
Este aminoácido es necesario para el correcto metabolismo de las grasas y ácidos grasos, el crecimiento del músculo, y el mantenimiento de un sistema inmunológico saludable. La Serina es un aminoácido que forma parte de las vainas de mielina protectora que cubre las fibras nerviosas, es importante para el funcionamiento del ARN y ADN y la formación de células y ayuda a la producción de inmunoglobulinas y anticuerpos.
Taurina
La Taurina fortalece el músculo cardíaco, mejora la visión, y ayuda a prevenir la degeneración macular, es el componente clave de la bilis, la cual es necesaria para la digestión de las grasas, útil para las personas con aterosclerosis, edema, trastornos del corazón, hipertensión o hipoglucemia. Es un aminoácido vital para la utilización adecuada de sodio, potasio, calcio y magnesio, ayuda a prevenir el desarrollo de arritmias cardiacas potencialmente peligrosas. La taurina se ha utilizado para tratar la ansiedad, epilepsia, hiperactividad, mal funcionamiento cerebral y convulsiones.
Tirosina
Es un aminoácido importante para el metabolismo general. La Tirosina es un precursor de la adrenalina y la dopamina, que regulan el estado de ánimo. Estimula el metabolismo y el sistema nervioso, actúa como un elevador del humor, suprime el apetito y ayuda a reducir la grasa corporal. La Tirosina ayuda en la producción de melanina (el pigmento responsable del color del pelo y la piel) y en las funciones de las glándulas suprarrenales, tiroides y la pituitaria, se ha utilizado para ayudar a la fatiga crónica, la narcolepsia, ansiedad, depresión, reducción de la líbido, alergias y dolores de cabeza.
miércoles, 2 de diciembre de 2015
Éter (química)
Éteres. Constituyen una clase de compuestos muy importantes debido a lo extraordinariamente difundido que se encuentra en la naturaleza. Los ésteres de peso molecular bajos son líquidos de olor agradables a frutas, mucho de los fragantes olores de los distintos frutos y flores se deben a los ésteres que contienen. Así, el acetato de isoamilo se encuentra en el plátano, el butirato de amilo en elalbaricoque, y el acetato de etilo en la piña tropical.
Por otra parte los ésteres de los ácidos alifáticos lineales de cadena larga constituyen los aceites,grasas y ceras que tanto abundan en los reinos vegetal y animal.
Contenido
[ocultar]Características
La mayoría de los éteres son líquidos volátiles, ligeros e inflamables, solubles en alcoholes y otros disolventes orgánicos. Desde el punto de vista químico, son compuestos inertes y estables; los álcalis o losácidos no los atacan fácilmente. Están estrechamente relacionados con los alcoholes y se obtienen directamente de ellos. El compuesto más típico y más utilizado de este grupo es el éter común o eter etílico, normalmente denominado éter.
Se les puede considerar el resultado de sustituir elhidrógeno del grupo OH de los alcoholes por un radical hidrocarbonado. Según el tipo de estos radicales, los éteres pueden ser:- Alifáticos, R—O—R (los dos radicales alquílicos).
- Aromáticos, Ar—O—Ar (los dos radicales arílicos).
- Mixtos, R—O—Ar (un radical alquílico y otro arílico).
Los éteres se llaman simétricos cuando los dos radicales son iguales y, asimétricos, si son distintos.
Nomenclatura
Para nombrar los éteres tenemos dos alternativas:- Primera: Considerar el grupo alcoxi como un sustituyente (siendo R el radical más sencillo).
- Segunda: Citar los dos radicales que están unidos al O por orden alfabético y a continuación la palabra éter.
Propiedades
Propiedades Químicas
Los éteres tienen muy poca reactividad química, debido a la dificultad que presenta la ruptura del enlace C—O. Por ello, se utilizan mucho como disolventes inertes en reacciones orgánicas. En contacto con el aire sufren una lenta oxidación en la que se forman peróxidos muy inestables y poco volátiles. Estos constituyen un peligro cuando se destila un éter, pues se concentran en el residuo y pueden dar lugar a explosiones. Esto se evita guardando el éter con hilo de sodio o añadiendo una pequeña cantidad de un reductor (SO4Fe, LiAIH4) antes de la destilación .
Propiedades Físicas
Estructuralmente los éteres pueden considerarse derivados del agua o alcoholes, en los que se han reemplazado uno o dos hidrógenos, respectivamente, por restos carbonados.
La estructura angular de los éteres se explica bien asumiendo una hibridación sp3 en el oxígeno, que posee dos pares de electrones no compartidos. No puede establecer enlaces de hidrógeno consigo mismo y sus puntos de ebullición y fusión son muchos más bajos que los alcoholes referibles. Un caso muy especial lo constituyen los epóxidos, que son éteres cíclicos de tres miembros. El anillo contiene mucha tensión, aunque algo menos que en elciclopropano.
Pero la presencia del oxígeno, que polariza los enlaces, y la existencia de la tensión, hace que los epóxidos, al contrario que los éteres normales, sean muy reactivos y extremadamente útiles en síntesis.
Debido a que el ángulo del enlace C-o-C no es de 180º, los momentos dipolares de los dos enlaces C-O no se anulan; en consecuencia, los éteres presentan un pequeño momento dipolar neto (por ejemplo, 1.18 D para el dietil éter).
Esta polaridad débil no afecta apreciablemente a los puntos de ebullición de los éteres, que son similares a los de los alcanos de pesos moleculares comparables y mucho más bajos que los de los alcoholes isómeros. Comparemos, por ejemplo, los puntos de ebullición del n-heptano (98ºC), el metil n-pentil éter (100ºC) y el alcohol hexílico (157ºC). Los puentes de hidrógeno que mantienen firmemente unidas las moléculas de alcoholes no son posibles para los éteres, pues éstos sólo tienen hidrógeno unido a carbono.
Por otra parte, los éteres presentan una solubilidad en agua comparable a la de los alcoholes: tanto el dietil éter como el alcohol n-butílico, por ejemplos, tienen una solubilidad de unos 8 g por 100g de agua. La solubilidad de los alcoholes inferiores se debe a los puentes de hidrógeno entre moléculas de agua y de alcohol; es probable que la solubilidad de los éteres en agua se debe a la misma causa.
Reacciones
Los éteres no son reactivos a excepción de los epóxidos.Las reacciones de los epóxidos pasan por la apertura del ciclo.Dicha apertura puede ser catalizada por ácido o apertura mediante nucleófilo.
Apertura catalizada por ácido
El nucleófilo ataca al carbono más sustituido.
Apertura por nucleófilo
El nucleófilo ataca al carbono menos sustituido.
Obtención
Deshidratación de alcoholes
Los éteres alifáticos simétricos pueden obtenerse por deshidratación de alcoholes , mediante la acción del ácido sulfúrico. Este es uno de los métodos comerciales de preparación del éter ordinario, dietiléter, por lo que se llama frecuentemente éter sulfúrico.Se lleva a cabo tratando el alcohol con ácido sulfúrico a 140°. La deshidratación es intermolecular:
Este proceso se ve fácilmente afectado por reacciones secundarias, como la formación de sulfatos de alquilo (especialmente si baja la temperatura), y la formación de olefinas (especialmente si sube la temperatura). La deshidratación de alcoholes puede también realizarse en fase vapor, sobre alúmina a 300°, aunque este procedimiento sólo es satisfactorio con alcoholes primarios, ya que los secundarios y los terciarios dan lugar a la formación de olefinas.
A partir de Alcoholatos
Este método también es conocido como Síntesis de Williamson. Los alcoholatos dan lugar a la formación de éteres al ser tratados con halogenuros de alquilo según:
Tipos de éteres
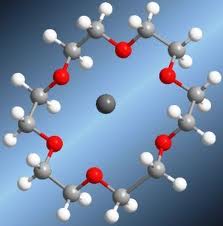
Éteres corona: Hay éteres que contienen más de un grupo funcional éter (poliéteres) y algunos de éstos forman ciclos; estos poliéteres se denominan éteres corona. Pueden sintetizarse de distintos tamaños y se suelen emplear como ligandos, para acomplejar selectivamente (por el tamaño) a cationes alcalinos. Los oxígenos establecen interacciones con el catión, que se coloca en el centro del ciclo, formándose un complejo. Existen en la naturaleza compuestos de este tipo. Suelen servir como transporte de cationes alcalinos para que puedan atravesar las membranas celulares y de esta forma matener las concentraciones óptimas a ambos lados. Por esta razón se pueden emplear como antibióticos, como por ejemplo, la valinomicina. Otros compuestos relacionados son los criptatos, que contienen, además de átomos de oxígeno, átomos de nitrógeno. A los criptatos y a los éteres corona se les suele denominar ionóforos.
Poliéteres: Se pueden formar polímeros que contengan el grupo funcional éter. Un ejemplo de formación de estos polímeros: R-OH + n(CH2)O ! R-O-CH2-CH2-O-CH2-CH2-O-CH2-CH2-O-.. Los poliéteres más conocidos son las resinas epoxi, que se emplean principalmente como adhesivos. Se preparan a partir de un epóxido y de un dialcohol.
Epóxidos u oxiranos: Los epóxidos u oxiranos son éteres en donde el átomo de oxígeno es uno de los átomos de un ciclo de tres. Son pues compuestos heterocíclicos. Los ciclos de tres están muy tensionados, por lo que reaccionan fácilmente en reacciones de apertura, tanto con bases como con ácidos.
Éteres de silicio: Hay otros compuestos en los que el grupo funcional no es R-O-R', estando el oxígeno unido a dos carbonos, pero siguen siendo llamados éteres. Por ejemplo, los éteres de silicio, en donde la fórmula general es R-O-Si, es decir, el oxígeno está unido a un carbono y a un átomo de silicio. Sigue habiendo un par de electrones no enlazantes. Estos compuestos se llaman éteres de silicio.
Aplicación
Son múltiples las aplicaciones que tienen estos compuestos. La más utilizada es como disolventes de aceites y grasas. Otras de sus aplicaciones son: Anestésico general. Medio extractar para concentrar ácido acético y otros ácidos. Medio de arrastre para la deshidratación de alcoholes etílicos e isopropílicos. Disolvente de sustancias orgánicas (aceites, grasas, resinas, nitrocelulosa, perfumes y alcaloides). Combustible inicial de motores Diesel.
Fuentes
- Bonner WA, Castro AJ. Química Orgánica Básica. 2 ed. La Habana; Editorial Pueblo y Revolución. 1979
- quimicaorganica.org
- Babor JA. Química General Moderna. 1ra reimpresión, Editorial Pueblo y Educación. 1978
- Durán Rivas Yunior, Ing Químico. Apuntes de Química. Santiago de Cuba, Cuba, año 2000
lunes, 23 de noviembre de 2015
jueves, 19 de noviembre de 2015
sábado, 14 de noviembre de 2015
USOS DE LOS ÁCIDOS ORGANICOS
Principales aplicaciones de los ácidos carboxílicos
¿Conoce las diferentes clases de ácidos carboxílicos? ¿Qué aplicaciones tienen?
Tema: Principales aplicaciones de los ácidos carboxílicos
A los compuestos que contienen el grupo carboxilo (abreviado -COOH o CO2H) se les denomina ácidos carboxílicos. El grupo carboxilo es el origen de una serie de compuestos orgánicos entre los que se encuentran los haluros de ácido (RCOCl), los anhidridos de ácido (RCOOCOR), los ésteres (RCOOR´), y las amidas (RCONH2).
Algunos ácidos carboxílicos muy utilizados en la industria son:
Ácido acrílico
Nombre común del ácido propénico. Este compuesto orgánico es un líquido incoloro, inflamable, cáustico y de olor punzante, con una temperatura de ebullición de 142 ºC. El ácido acrílico es el ácido carboxílico insaturado más sencillo; sus sales y ésteres se denominan acrilatos. Su reacción principal es la polimerización: los poliacrilatos resultantes son a menudo transparentes pero quebradizos. Para modificar sus propiedades físicas y químicas, pueden combinarse con otros componentes (copolimerización). Así, el ácido acrílico es el material de partida para fabricar plásticos, barnices, resinas elásticas y adhesivos transparentes. Para más información haga click aquí
Ácido benzoico
Sólido de fórmula C6H5—COOH, poco soluble en agua y de acidez ligeramente superior a la de los ácidos alifáticos sencillos. Se usa como conservador de alimentos. Es poco tóxico y casi insípido. El ácido benzoico se combina con el ácido salicílico en forma de pomada con propiedades antimicóticos. Puede aplicarse sin peligro a la piel. Para más información haga click aquí
Ácido fumárico
Acido trans-butenodioico, compuesto cristalino incoloro, de fórmula HO2CCH=CHCO2H, que sublima a unos 200 °C. Se encuentra en ciertos hongos y en algunas plantas, a diferencia de su isómero cis, el ácido maleico (cis-butenodioico), que no se produce de forma natural.
Se utiliza en el procesado y conservación de los alimentos por su potente acción antimicrobiana, y para fabricar pinturas, barnices y resinas sintéticas. Para más información haga click aquí
Ácido linoleico
Líquido oleoso, incoloro o amarillo pálido, de fórmula CH3(CH2)4(CH=CHCH2)2(CH2)6CO2H, cuyos dobles enlaces presentan configuración cis. Es soluble en disolventes orgánicos y se polimeriza con facilidad, lo que le confiere propiedades secantes. El ácido linoleico es un ácido graso esencial, es decir, es un elemento necesario en la dieta de los mamíferos por ser uno de los precursores de las prostaglandinas y otros componentes de tipo hormonal.
Se encuentra como éster de la glicerina en muchos aceites de semillas vegetales, como los de linaza, soja, girasol y algodón. Se utiliza en la fabricación de pinturas y barnices. Para más información haga click aquí
Ácido oleico
Líquido oleoso e incoloro, de fórmula CH3(CH2)7CH=CH(CH2)7CO2H en su configuración cis (la cadena de carbono continúa en el mismo lado del doble enlace). Es un ácido graso no saturado que amarillea con rapidez en contacto con el aire. Por hidrogenación del ácido oleico se obtiene el ácido esteárico (saturado). No es soluble en agua, pero sí en benceno, alcohol, éter y otros muchos disolventes orgánicos. Se solidifica por enfriamiento y funde a 14 °C. Su isómero trans (ácido elaídico) es sólido y funde a 51 °C; se puede obtener por calentamiento del ácido oleico en presencia de un catalizador.
Junto con el ácido esteárico y el ácido palmítico se encuentra, en forma de éster, en la mayoría de las grasas y aceites naturales, sobre todo en el aceite de oliva. Se obtiene por hidrólisis del éster y se purifica mediante destilación. Se utiliza en la fabricación de jabones y cosméticos, en la industria textil y en la limpieza de metales.Para más información haga click aquí
Ácido salicílico
Sólido blanco y cristalino, que se encuentra en numerosas plantas, en especial en los frutos, en forma de metilsalicilato, y se obtiene comercialmente a partir del fenol.
Tiene un sabor ligeramente dulce; es poco soluble en agua y más soluble en alcohol, éter y cloroformo. Tiene un punto de fusión de 159 °C. Este ácido se emplea sobre todo para preparar algunos ésteres y sales importantes. El salicilato de sodio, que se obtiene tratando el fenolato de sodio con dióxido de carbono a presión, se usa para preservar alimentos y en mayor medida para elaborar preparados antisépticos suaves como pasta de dientes y colutorios. Los compuestos salicílicos medicinales empleados como analgésicos y antipiréticos son el ácido acetilsalicílico y el fenilsalicilato, que se venden bajo el nombre comercial de aspirina y salol, respectivamente. El metilsalicilato es el principal componente del aceite de gaulteria o esencia de Wintergreen, y se fabrica sintéticamente en grandes cantidades por reacción de ácido salicílico y metanol. Para más información haga clickaquí
Ácido caprílico o Ácido undecilénico
Líquido amarillo de fórmula CH3(CH2)4COOH, con olor a rancio característico, de actividad fungicida contra diversos hongos. El ácido caprílico y sus sales presentan acción dermatomicótica. Para más información haga click aquí
Ácido esteárico
Sólido orgánico blanco de apariencia cristalina, de fórmula CH3(CH2)16COOH. No es soluble en agua, pero sí en alcohol y éter. Junto con los ácidos láurico, mirístico y palmítico, forma un importante grupo de ácidos grasos. Se encuentra en abundancia en la mayoría de los aceites y grasas, animales y vegetales, en forma de éster—triestearato de glicerilo o estearina— y constituye la mayor parte de las grasas de los alimentos y del cuerpo humano. El ácido se obtiene por la hidrólisis del éster, y comercialmente se prepara hidrolizando el sebo. Se utiliza en mezclas lubricantes, materiales resistentes al agua, desecantes de barnices, y en la fabricación de velas de parafina. Combinado con hidróxido de sodio el ácido esteárico forma jabón (estearato de sodio).
El ácido esteárico se emplea para combinar caucho o hule con otras sustancias, como pigmentos u otros materiales que controlen la flexibilidad de los productos derivados del caucho; también se usa en la polimerización de estireno y butadieno para hacer caucho artificial. Para más información haga click aquí
Ácido etanoico o Ácido acético
Líquido incoloro, de fórmula CH3 COOH, de olor irritante y sabor amargo. En una solución acuosa actúa como ácido débil. El ácido etanoico puro recibe el nombre de ácido etanoico glacial, debido a que se congela a temperaturas ligeramente más bajas que la ambiente. En mezclas con agua solidifica a temperaturas mucho más bajas. El ácido etanoico es miscible (mezclable) con agua y con numerosos disolventes orgánicos.
Las soluciones diluidas (de 4 a 8%) preparadas de este modo a partir del vino, sidra o malta constituyen lo que conocemos como vinagre. El ácido etanoico concentrado se prepara industrialmente mediante distintos procesos, como la reacción de metanol (alcohol metílico) y de monóxido de carbono (CO) en presencia de un catalizador, o por la oxidación del etanal (acetaldehído).
El ácido acético se utiliza en la producción de acetato de rayón, plásticos, películas fotográficas, disolventes para pinturas y medicamentos como la aspirina. Tiene un punto de ebullición de 118 °C y un punto de fusión de 17 °C.Para más información haga click aquí
Suscribirse a:
Entradas (Atom)